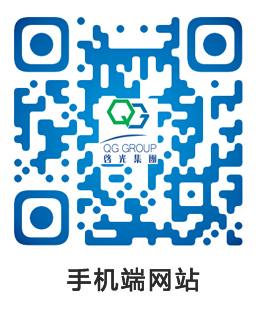
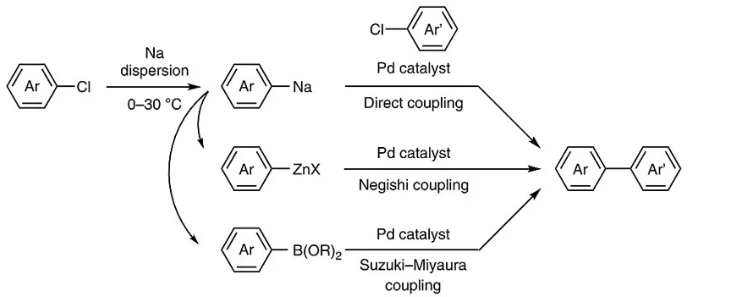
有機鈉化合物的製備。有機鈉化合物在Negishi和Suzuki–Miyaura反應中的應用通過上述方法製備的有機鈉化合物可以用ZnCl2•TMEDA(比ZnCl2對水汽穩定)進行轉金屬化得到有機鋅試劑,這樣要比通過溴代物或碘代...
有機鈉化合物在Negishi和Suzuki–Miyaura反應中的應用
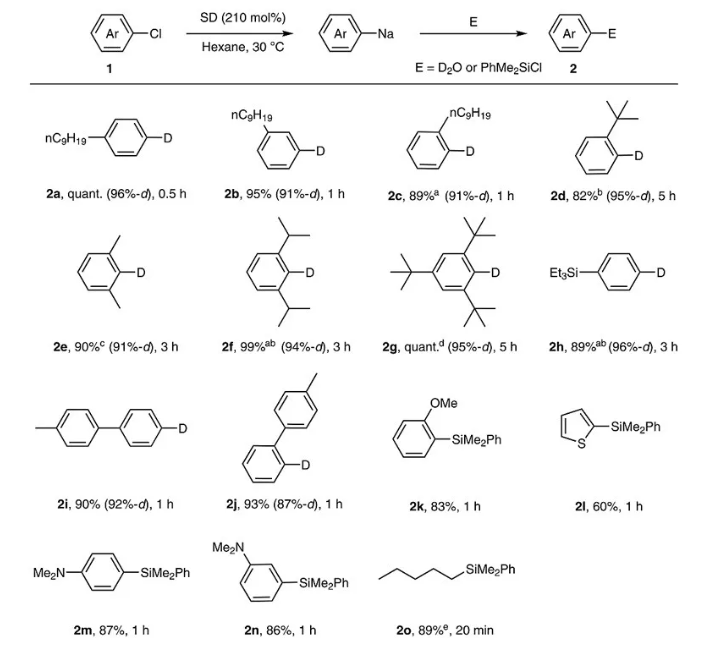
通過上述方法製備的有機鈉化合物可以用ZnCl2•TMEDA(比ZnCl2對水汽穩定)進行轉金屬化得到有機鋅試劑,這樣要比通過溴代物或碘代物去製備成本低很多,操作也更方便。後者在Valente等人開發的催化劑Pd-PEPPSI-IPr催化下可進一步與(yu) 另一分子的芳基氯代物發生Negishi偶聯。這種方法可以實現大位阻雙芳基化合物的“一鍋法”合成(3b-3g),反應對芳基氯代物的電子特性沒有特別的要求(3j、3o、3p和3s);敏感的官能團如烷氧基羰基(3i、3p、3t)或氰基(3u)都能很好地與(yu) 反應兼容。該反應的轉化數可高達920(0.1 mol%的催化劑,以92%的收率得到3i),甚至還能以克量級規模合成(如3i)。烷基氯代物(3r、3s)和烯基氯代物(3q)也能參與(yu) 反應。值得一提的是,芳香雜環類底物如苯並呋喃和苯並噻吩可以在NaTMP(TMP:2,2,6,6-四甲基呱啶)作用下直接去質子化得到相應的芳基鈉化合物,進而發生Negishi反應(3t、3u)。
有機鈉化合物參與(yu) 的Negishi反應。
同理,這些芳基鈉化合物與(yu) 硼酸酯(如MeOBpin、B(OMe)3和i-PrOBpin)反應可轉化成相應的芳基硼酸酯,後者再在Pd-PEPPSI-IPr催化下可與(yu) 另一分子芳基氯代物發生Suzuki–Miyaura反應得到二芳基化合物。值得說明的是,這一反應也可以實現“一鍋法”並且不需要外源堿的添加,因為(wei) 芳基鈉和MeOBpin反應就能釋放NaOMe,而且略過量的鈉/石蠟油分散體(ti) 會(hui) 與(yu) 偶聯反應中加入的水反應生成NaOH。
芳基鈉化合物參與(yu) 的Suzuki–Miyaura反應
芳基鈉直接用於(yu) 芳基鹵代物的交叉偶聯
Fañanás–Mastral等人已經發現2,6-二甲氧基苯基鋰可以在Pd-PEPPSI-IPent催化下與(yu) 1-萘基溴在室溫下偶聯,以94%的收率得到5a。因此,研究人員也將製備的芳基鈉化合物進行同樣的反應,發現其都能與(yu) 另一分子的芳基氯代物或溴代物以很高的收率得到二芳基化合物(除了對甲基氯苯)。如果沒有催化劑存在,反應也能得到少量產(chan) 物,可能是經曆了苯炔中間態導致產(chan) 物以區域異