水氧穩定的固體(ti) 炔基鋅試劑的合成與(yu) 應用雙取代炔烴在材料科學和藥物化學中具有廣泛的應用前景,同時也是合成含有多官能團烯烴的重要前體(ti) ,以炔基金屬試劑為(wei) 原料與(yu) 不同親(qin) 電試劑反應是得到多取代炔烴的主要方法...
水氧穩定的固體(ti) 炔基鋅試劑的合成與(yu) 應用
雙取代炔烴在材料科學和藥物化學中具有廣泛的應用前景,同時也是合成含有多官能團烯烴的重要前體(ti) ,以炔基金屬試劑為(wei) 原料與(yu) 不同親(qin) 電試劑反應是得到多取代炔烴的主要方法之一。目前,已有多篇文獻報道了通過芳香(雜)環、烯丙基和苄基鹵代物製備得到對水氧穩定的有機金屬試劑,其中有機鋅試劑在高通量篩選生物活性分子中具有很好的前景,固相的Reformatsky烯醇化反應已經能夠很好地應用於(yu) 有機反應中。此外,芳香(雜)環鋅試劑因在空氣中可以存在,在Co催化的偶聯反應中使用廣泛。最近,來自德國慕尼黑大學的Paul Knochel教授課題組報道了一類新的水氧穩定的炔基鋅試劑的合成,並以此出發成功合成了雙取代的炔烴。
作者通過末端炔與(yu) TMPZnCl•Mg(OPiv)2(3,TMP=2,2,6,6-四甲基呱啶)合成了炔基鋅試劑(1),對多種官能團都具有很好地兼容性。初步研究表明,三甲基矽基乙炔(2a)與(yu) TMPZnOPiv•LiCl反應可以得到炔基鋅試劑1a,但其穩定性較差(空氣中放置4 h後僅(jin) 保留44%的活性),他們(men) 猜測LiCl的存在可能導致鋅試劑的穩定性較差。隨後他們(men) 使用苄基格氏試劑與(yu) TMPH在THF中反應,然後加入Zn(OPiv)2,可以定量得到TMPZnOPiv(3),3與(yu) 2a反應可以得到炔基鋅試劑1a,並且在空氣中放置4 h後,仍然得到90%的收率(圖1)。通過這一方法,作者可以製備含有羰基、氰基、酯基等官能團的炔基鋅試劑,這類試劑在空氣中放置4 h後仍然具有43-90%的反應活性。
炔基鋅試劑的合成。圖片來源:Angew. Chem. Int. Ed.

接下來,他們(men) 將製備的炔基鋅試劑應用到Negishi偶聯反應中。通過條件篩選,作者最終確定Pd(dba)2與(yu) DavePhos配體(ti) 結合具有最好的催化活性,在此條件下,一係列的芳香(雜)環碘代物、溴代物、氯代物都能夠與(yu) 炔基鋅試劑發生反應得到目標產(chan) 物;此外,酯基、酰基、甲氧基、氰基、二級胺、酰胺等基團都具有良好的兼容性,並且芳香雜環修飾的炔基鋅試劑參與(yu) 反應也具有理想的收率。
炔基鋅試劑1的Negishi偶聯。圖片來源:Angew. Chem. Int. Ed.

該類炔基鋅試劑也可以參與(yu) 到其他過渡金屬催化的偶聯反應中。炔基鋅試劑1e與(yu) 硫代羧酸酯7在Pd催化下可以得到炔基酮8;1j與(yu) 烯丙基溴9經由CuCN•2LiCl催化可以得到烯炔10;1c可以對醛親(qin) 核加成得到炔丙基醇。
炔基鋅試劑的其他偶聯反應。圖片來源:Angew. Chem. Int. Ed.
除此之外,他們(men) 發現炔基鋅試劑也可以發生Cu催化的Click反應(CuAAC),區域選擇性地得到1,4-二取代三唑(圖4)。炔基鋅試劑1可以與(yu) 芳基疊氮化物或者原位產(chan) 生的苄基疊氮化物(苄基溴與(yu) NaN3反應製備)在CuI催化下得到三唑的鋅試劑,與(yu) 親(qin) 電試劑偶聯得到多取代的1,2,3-三唑(6a-d)。
Cu催化的1,3-偶極環加成反應。圖片來源:Angew. Chem. Int. Ed.
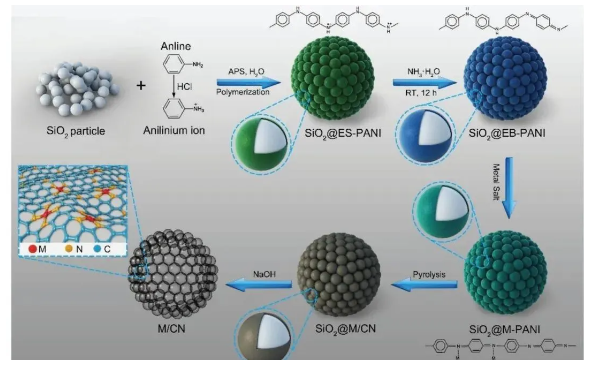
在此基礎之上,他們(men) 還將該反應應用到具有潛在抗腫瘤活性藥物18的合成中,化合物22與(yu) NaN3反應原位得到苄基疊氮化物,與(yu) 炔基鋅試劑1d偶聯得到關(guan) 鍵三唑類中間體(ti) 23,經過後續反應得到最終產(chan) 物18
羧胺三唑18的合成。圖片來源:Angew. Chem. Int. Ed.
Paul Knochel教授課題組報道了一種合成炔基鋅試劑的新方法,該試劑對水氧具有良好的穩定性以及官能團兼容性,並可應用於(yu) 與(yu) 多種芳基、烷基和酰基的偶聯反應。該類鋅試劑同時也可以進行Cu催化的1,3-偶極環加成反應,並且在反應中保留C-Zn鍵。他們(men) 通過Click反應還可以得到藥物分子18,該試劑在藥物合成中具有很好的應用前景。